Legea lui Boyle (numită și legea lui Mariotte și legea Boyle-Mariotte) este o lege despre gazele ideale.
Legea poate fi enunțată după cum urmează:
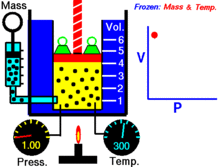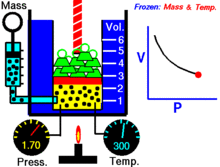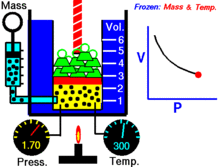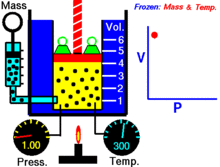
Pentru o cantitate fixă de gaz ideal, menținută la o temperatură fixă, P (presiune) și V (volum) sunt invers proporționale.
Cu alte cuvinte, volumul unei mase constante de gaz ideal la o temperatură constantă este invers proporțional cu presiunea aplicată asupra acestuia.
În simboluri, legea este:
P ∝ 1 V {\displaystyle P\propto {\frac {1}{V}}}
sau
P V = k {\displaystyle PV=k}
unde P este presiunea gazului, V este volumul gazului, iar k este o constantă.
Pentru o anumită masă de gaz la o temperatură constantă, produsul dintre presiune și volum este o constantă. Pe măsură ce volumul scade, presiunea crește proporțional și invers. De exemplu, când presiunea se înjumătățește, volumul se dublează.
Să presupunem că aveți un rezervor care conține un anumit volum de gaz la o anumită presiune. Atunci când reduceți volumul rezervorului, același număr de particule de gaz este acum conținut într-un spațiu mai mic. Prin urmare, numărul de coliziuni crește. Prin urmare, presiunea este mai mare.
Imaginați-vă că aveți un gaz la o anumită presiune (P1) și un anumit volum (V1). Dacă modificați presiunea la o nouă valoare (P2), volumul se modifică la o nouă valoare (V2). Putem folosi legea lui Boyle pentru a descrie ambele seturi de condiții:
P 1 V 1 = k {\displaystyle P_{1}V_{1}=k}
P 2 V 2 = k {\displaystyle P_{2}V_{2}=k}
Constanta, k, este aceeași în ambele cazuri, astfel încât putem spune următoarele:
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}
Exemplu: Presiunea unui gaz este de 3 atm, iar volumul este de 5 litri. Dacă presiunea este redusă la 2 atm, care este volumul?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}
V 2 = P 1 V 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}{P_{2}}}}
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={\frac {3*5}{2}}}}
V 2 = 15 2 {\displaystyle V_{2}={\frac {15}{2}}}}
V 2 = 7.5 {\displaystyle V_{2}=7.5}
∴ Volumul va fi de 7,5 litri.
Legea a fost găsită de Robert Boyle în 1662, iar apoi, în mod independent, de Edme Mariotte în 1679.