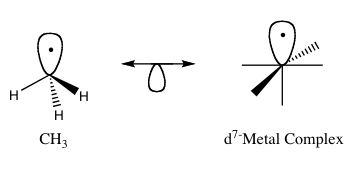
Principiul izolobal (cunoscut și sub numele de analogie izolobală) este o modalitate de a prezice proprietățile de legătură ale compușilor organometalici. În chimia organometalică, acesta se referă la structura liganzilor organici care se pot lega de fragmente moleculare anorganice. Roald Hoffmann a descris fragmentele moleculare ca fiind isolobe "dacă numărul, proprietățile de simetrie, energia aproximativă și forma orbitalilor de frontieră și numărul de electroni din aceștia sunt similare - nu identice, dar similare". Se poate prezice legătura și reactivitatea unor fragmente mai puțin cunoscute de la cele ale unor fragmente mai bine cunoscute dacă cele două fragmente moleculare au orbitali de frontieră similari, cel mai înalt orbital molecular ocupat (HOMO) și cel mai mic orbital molecular neocupat (LUMO). Compușii izolobali sunt analogii ai compușilor izoelectronici care au în comun același număr de electroni de valență și aceeași structură. O reprezentare grafică a structurilor izolobe, cu perechile izolobe conectate printr-o săgeată cu două capete cu jumătate de orbital dedesubt, se găsește în figura 1.
Pentru activitatea sa privind analogia izolobală, Hoffmann a primit Premiul Nobel pentru Chimie în 1981, pe care l-a împărțit cu Kenichi Fukui. În discursul său de decernare a Premiului Nobel, Hoffmann a subliniat că analogia isolobală este un model util, dar simplu. Ea eșuează în anumite cazuri.