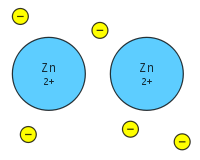
O legătură metalică este împărțirea mai multor electroni detașați între mai mulți ioni pozitivi, unde electronii acționează ca un "lipici" care conferă substanței o structură definită. Ea este diferită de legătura covalentă sau ionică. Metalele au o energie de ionizare scăzută. Prin urmare, electronii de valență pot fi delocalizați în toate metalele. Electronii delocalizați nu sunt asociați cu un anumit nucleu al unui metal, în schimb, ei sunt liberi să se deplaseze în întreaga structură cristalină, formând o "mare" de electroni.
Electronii și ionii pozitivi din metal au o forță de atracție puternică între ei. Prin urmare, metalele au adesea un punct de topire sau de fierbere ridicat. Principiul este similar cu cel al legăturilor ionice.
Legăturile metalice determină multe dintre trăsăturile metalelor, cum ar fi rezistența, maleabilitatea, ductilitatea, strălucirea, conducerea căldurii și a electricității.
Deoarece electronii se mișcă liber, metalul are o anumită conductivitate electrică. Aceasta permite ca energia să treacă rapid prin electroni, generând un curent electric. Metalele conduc căldura din același motiv: electronii liberi pot transfera energia cu o viteză mai mare decât alte substanțe cu electroni care sunt fixați în poziție. Există, de asemenea, câteva nemetale care conduc electricitatea: grafitul (deoarece, la fel ca și metalele, are electroni liberi) și compușii ionici care sunt topiți sau dizolvați în apă, care au ioni liberi în mișcare.
Legăturile metalice au cel puțin un electron de valență pe care nu îl împart cu atomii vecini și nu pierd electroni pentru a forma ioni. În schimb, nivelurile energetice exterioare (orbitali atomici) ale atomilor de metal se suprapun. Ele sunt similare legăturilor covalente. Nu toate metalele prezintă legături metalice. De exemplu, ionii de mercur (Hg2+
2) formează legături metal-metal covalente.
Un aliaj este o soluție de metale. Cele mai multe aliaje sunt strălucitoare, la fel ca și metalele pure.