Legăturile covalente sunt legături chimice între doi atomi nemetalici. Un exemplu este apa, unde hidrogenul (H) și oxigenul (O) se leagă împreună pentru a forma (H2O). Un înveliș exterior complet are, de obicei, opt electroni, sau doi în cazul hidrogenului sau al heliului. Electronii de valență sunt electronii ținuți relativ liber în învelișul exterior al atomului. Structura învelișurilor de electroni este determinată de mecanica cuantică).
Numărul de electroni dintr-un atom este determinat de numărul de protoni din atom. Electronii orbitează în jurul nucleelor atomice și sunt ca niște traiectorii orbitale neclare în jurul unui nucleu atomic. Primul strat are până la doi electroni. Straturile următoare conțin, de obicei, până la opt. Legăturile covalente sunt formate prin partajarea electronilor de valență de către atomi.
Dacă, de exemplu, un atom ar avea nouă electroni, primii doi ar orbita foarte aproape de nucleu, iar următorii șapte ar orbita puțin mai departe. Cei șapte electroni din exterior sunt mai puțin strânși decât cei doi electroni din interior, deoarece sunt mai departe de nucleul încărcat pozitiv. Dacă acest atom se apropie de un alt atom, cu un electron slab reținut în învelișul său exterior, un nou orbital va deveni disponibil pentru electronul slab reținut. Acest nou orbital al electronului este legat de ambele nuclee atomice și are un nivel de energie mai mic decât orbitalul original al electronului. Electronul poate sări în mod spontan în acest orbital și poate emite un foton cu energia în exces. Acum avem un electron care orbitează în jurul ambilor atomi, ceea ce face ca atomul care a furnizat electronul să aibă o mică sarcină pozitivă netă, iar celălalt atom să aibă o mică sarcină negativă netă. Cei doi atomi sunt acum ținuți împreună de forța electromagnetică de atracție dintre sarcinile pozitive și negative. Aceasta se numește legătură covalentă. Pentru a rupe această legătură este nevoie de aceeași cantitate de energie care a fost eliberată în momentul formării ei.
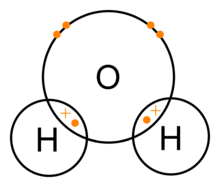
O moleculă de apă este formată dintr-un atom de oxigen și doi atomi de hidrogen, care sunt ținuți împreună printr-o legătură covalentă. În acest caz, atomul de oxigen împarte câte un electron cu fiecare atom de hidrogen. Acest lucru înseamnă că atomul de oxigen are o mică sarcină pozitivă netă, iar atomul de hidrogen are o mică sarcină negativă netă. Ca urmare, atomii de oxigen și de hidrogen sunt atrași unul de celălalt datorită forței electromagnetice. Din acest motiv, molecula de apă este o moleculă polară: sarcina sa nu este distribuită uniform.