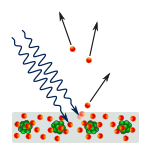
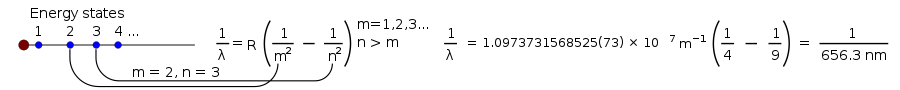Formulele și ideile mecanicii cuantice au fost create pentru a explica lumina care provine de la hidrogenul incandescent. De asemenea, teoria cuantică a atomului trebuia să explice de ce electronul rămâne pe orbita sa, ceea ce alte idei nu reușeau să explice. Din ideile mai vechi reieșea că electronul ar trebui să cadă în centrul atomului, deoarece la început este menținut pe orbită de propria sa energie, dar își pierde rapid energia pe măsură ce se rotește pe orbită. (Acest lucru se datorează faptului că se știa că electronii și alte particule încărcate emit lumină și pierd energie atunci când își schimbă viteza sau se rotesc).
Lămpile cu hidrogen funcționează la fel ca lămpile cu neon, dar lămpile cu neon au propriul lor grup unic de culori (și frecvențe) de lumină. Oamenii de știință au aflat că pot identifica toate elementele după culorile de lumină pe care le produc. Doar că nu și-au putut da seama cum se determină frecvențele.
Apoi, un matematician elvețian pe nume Johann Balmer a descoperit o ecuație care indica valoarea lui λ (lambda, pentru lungimea de undă):
λ = B ( n 2 n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\left({\frac {n^{2}}{n^{2}-4}}\right)\qquad \qquad \qquad n=3,4,5,6} 
unde B este un număr pe care Balmer l-a determinat ca fiind egal cu 364,56 nm.
Această ecuație a funcționat numai pentru lumina vizibilă emisă de o lampă cu hidrogen. Dar, mai târziu, ecuația a devenit mai generală:
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {\frac {1}{\lambda }}=R\left({\frac {1}{m^{2}}}-{\frac {1}{n^{2}}}\right),} 
unde R este constanta Rydberg, egală cu 0,0110 nm−1 , iar n trebuie să fie mai mare decât m.
Introducând numere diferite pentru m și n, este ușor de prezis frecvențele pentru multe tipuri de lumină (ultravioletă, vizibilă și infraroșie). Pentru a vedea cum funcționează acest lucru, mergeți la Hyperphysics și coborâți dincolo de mijlocul paginii. (Folosiți H = 1 pentru hidrogen).
În 1908, Walter Ritz a realizat principiul combinației Ritz, care arată cum anumite intervale între frecvențe se repetă. Acest lucru s-a dovedit a fi important pentru Werner Heisenberg câțiva ani mai târziu.
În 1905, Albert Einstein a folosit ideea lui Planck pentru a demonstra că un fascicul de lumină este alcătuit dintr-un flux de particule numite fotoni. Energia fiecărui foton depinde de frecvența sa. Ideea lui Einstein reprezintă începutul ideii din mecanica cuantică potrivit căreia toate particulele subatomice, cum ar fi electronii, protonii, neutronii și altele, sunt atât unde, cât și particule în același timp. (Vezi imaginea atomului cu electronul ca undă la atom.) Acest lucru a dus la o teorie despre particulele subatomice și undele electromagnetice numită dualitatea undă-particulă. Aceasta constă în faptul că particulele și undele nu erau nici una, nici cealaltă, ci aveau anumite proprietăți ale ambelor.
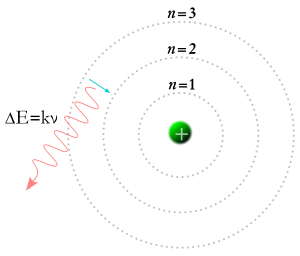
În 1913, Niels Bohr a venit cu ideea că electronii pot ocupa doar anumite orbite în jurul nucleului unui atom. Conform teoriei lui Bohr, numerele numite m și n din ecuația de mai sus ar putea reprezenta orbite. Conform teoriei lui Bohr, electronii ar putea începe pe o anumită orbită m și ar putea ajunge pe o anumită orbită n, sau un electron ar putea începe pe o anumită orbită n și ar putea ajunge pe o anumită orbită m, astfel încât, dacă un foton lovește un electron, energia acestuia va fi absorbită, iar electronul se va deplasa pe o orbită superioară datorită energiei suplimentare. Conform teoriei lui Bohr, dacă un electron cade de pe o orbită superioară pe o orbită inferioară, atunci va trebui să cedeze energie sub forma unui foton. Energia fotonului va fi egală cu diferența de energie dintre cele două orbite, iar energia unui foton îl face să aibă o anumită frecvență și culoare. Teoria lui Bohr a oferit o explicație bună pentru multe aspecte ale fenomenelor subatomice, dar nu a reușit să răspundă de ce fiecare dintre culorile luminii produse de hidrogenul incandescent (și de neon sau de orice alt element incandescent) are o luminozitate proprie, iar diferențele de luminozitate sunt întotdeauna aceleași pentru fiecare element.
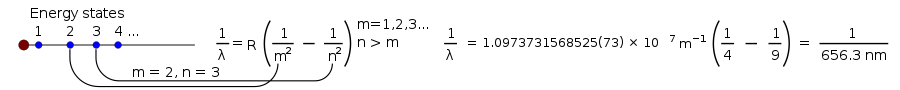
În momentul în care Niels Bohr a prezentat teoria sa, se cunoșteau cele mai multe lucruri despre lumina produsă de o lampă cu hidrogen, dar oamenii de știință încă nu puteau explica luminozitatea fiecărei linii produse de hidrogenul incandescent.
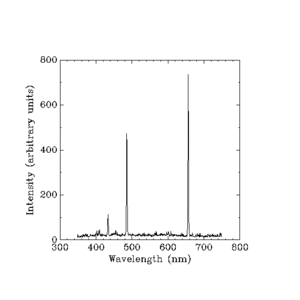
Werner Heisenberg a preluat sarcina de a explica luminozitatea sau "intensitatea" fiecărei linii. El nu a putut folosi nicio regulă simplă precum cea pe care o inventase Balmer. El a trebuit să folosească matematica foarte dificilă a fizicii clasice care calculează totul în termeni de lucruri precum masa (greutatea) unui electron, sarcina (puterea electrică statică) a unui electron și alte cantități minuscule. Fizica clasică avea deja răspunsuri pentru luminozitatea benzilor de culoare pe care le produce o lampă cu hidrogen, dar teoria clasică spunea că ar trebui să existe un curcubeu continuu, și nu patru benzi de culoare separate. Explicația lui Heisenberg este următoarea:
Există o lege care spune ce frecvențe de lumină va produce hidrogenul incandescent. Ea trebuie să prezică frecvențe distanțate atunci când electronii implicați se deplasează între orbite apropiate de nucleul (centrul) atomului, dar trebuie să prezică și faptul că frecvențele se vor apropia din ce în ce mai mult pe măsură ce observăm ce face electronul în deplasarea între orbite din ce în ce mai îndepărtate. De asemenea, va prezice că diferențele de intensitate dintre frecvențe se apropie din ce în ce mai mult pe măsură ce ne îndepărtăm. Acolo unde fizica clasică oferă deja răspunsurile corecte printr-un set de ecuații, noua fizică trebuie să ofere aceleași răspunsuri, dar prin ecuații diferite.
Fizica clasică folosește metodele matematice ale lui Joseph Fourier pentru a face o imagine matematică a lumii fizice, folosind colecții de curbe netede care se unesc pentru a forma o singură curbă lină care oferă, în acest caz, intensități pentru lumina de toate frecvențele de la o anumită lumină. Dar nu este corect, deoarece această curbă netedă apare doar la frecvențe mai mari. La frecvențe mai mici, există întotdeauna puncte izolate și nimic nu leagă punctele. Așadar, pentru a realiza o hartă a lumii reale, Heisenberg a trebuit să facă o mare schimbare. A trebuit să facă ceva pentru a selecta doar numerele care să corespundă cu ceea ce se vedea în natură. Uneori, oamenii spun că a "ghicit" aceste ecuații, dar el nu a făcut presupuneri oarbe. El a găsit ceea ce avea nevoie. Numerele pe care le-a calculat ar fi pus puncte pe un grafic, dar nu ar fi existat nicio linie trasată între puncte. Iar realizarea unui "grafic" format doar din puncte pentru fiecare set de calcule ar fi irosit multă hârtie și nu ar fi dus la nimic. Heisenberg a găsit o modalitate de a prezice în mod eficient intensitățile pentru diferite frecvențe și de a organiza aceste informații într-un mod util.
Folosind doar regula empirică dată mai sus, cea pe care Balmer a început-o și Rydberg a îmbunătățit-o, putem vedea cum să obținem un set de numere care l-ar ajuta pe Heisenberg să obțină tipul de imagine pe care și-o dorea:
Regula spune că, atunci când electronul se deplasează de pe o orbită pe alta, acesta câștigă sau pierde energie, în funcție de faptul că se îndepărtează sau se apropie de centru. Astfel, putem pune aceste orbite sau niveluri de energie sub formă de rubrici de-a lungul părții superioare și laterale a unei grile. Din motive istorice, cea mai joasă orbită se numește n, iar următoarea orbită se numește n - a, apoi vine n - b și așa mai departe. Este derutant faptul că s-au folosit numere negative atunci când electronii câștigau de fapt energie, dar așa stau lucrurile.
Deoarece regula lui Rydberg ne oferă frecvențe, putem folosi această regulă pentru a introduce numere în funcție de locul unde se duce electronul. Dacă electronul începe la n și sfârșește la n, atunci nu a plecat nicăieri, deci nu a câștigat energie și nici nu a pierdut energie. Așadar, frecvența este 0. Dacă electronul începe la n-a și ajunge la n, atunci a căzut de pe o orbită superioară pe o orbită inferioară. Dacă face acest lucru, atunci pierde energie, iar energia pe care o pierde apare sub forma unui foton. Fotonul are o anumită cantitate de energie, e, iar aceasta este legată de o anumită frecvență f prin ecuația e = h f. Așadar, știm că o anumită schimbare de orbită va produce o anumită frecvență a luminii, f. Dacă electronul începe la n și ajunge la n - a, înseamnă că a trecut de pe o orbită inferioară pe o orbită superioară. Acest lucru se întâmplă numai atunci când un foton cu o anumită frecvență și energie vine din exterior, este absorbit de electron și îi conferă energie, ceea ce face ca electronul să treacă pe o orbită superioară. Așadar, pentru ca totul să aibă sens, scriem această frecvență ca număr negativ. A existat un foton cu o anumită frecvență, iar acum a fost luat.
Deci, putem face o grilă ca aceasta, unde f(a←b) înseamnă frecvența implicată atunci când un electron trece de la starea energetică (orbita) b la starea energetică a (Din nou, secvențele arată invers, dar așa au fost scrise inițial.):
Grila de f
| Stări electronice | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| tranziție.... | ..... | ..... | ..... | ..... | | |
Heisenberg nu a făcut grilele în acest fel. El a făcut doar calculele matematice care să-i permită să obțină intensitățile pe care le căuta. Dar, pentru a face acest lucru, el a trebuit să înmulțească două amplitudini (cât de mare măsoară o undă) pentru a calcula intensitatea. (În fizica clasică, intensitatea este egală cu amplitudinea la pătrat.) A făcut o ecuație ciudată pentru a rezolva această problemă, a scris restul lucrării, i-a înmânat-o șefului său și a plecat în vacanță. Dr. Born s-a uitat la ecuația sa ciudată și i s-a părut puțin nebună. Probabil că s-a întrebat: "De ce mi-a dat Heisenberg chestia asta ciudată? De ce trebuie să o facă în felul acesta?". Apoi și-a dat seama că se uita la un plan pentru ceva ce știa deja foarte bine. El era obișnuit să numească matrice grila sau tabelul pe care îl puteam scrie făcând, de exemplu, toate calculele matematice pentru frecvențe. Iar ecuația ciudată a lui Heisenberg era o regulă pentru înmulțirea a două dintre ele. Max Born a fost un matematician foarte, foarte bun. El știa că, din moment ce cele două matrici (grile) care se înmulțesc reprezentau lucruri diferite (cum ar fi poziția (x,y,z) și impulsul (mv), de exemplu), atunci când înmulțești prima matrice cu a doua obții un răspuns, iar când înmulțești a doua matrice cu prima matrice obții un alt răspuns. Chiar dacă nu cunoștea matematica matricială, Heisenberg văzuse deja această problemă a "răspunsurilor diferite" și îl deranjase. Dar Dr. Born era un matematician atât de bun încât a văzut că diferența dintre prima înmulțire a matricei și a doua înmulțire a matricei va implica întotdeauna constanta lui Planck, h, înmulțită cu rădăcina pătrată a lui unu negativ, i. Astfel, la câteva zile după descoperirea lui Heisenberg, aveau deja matematica de bază pentru ceea ce lui Heisenberg îi plăcea să numească "principiul nedeterminării". Prin "nedeterminat", Heisenberg se referea la faptul că ceva precum un electron nu este fixat până când nu este fixat. Este un pic ca o meduză care se înghesuie mereu și nu poate fi "la un loc" decât dacă o omori. Mai târziu, oamenii au devenit obișnuiți să numească acest principiu "principiul incertitudinii lui Heisenberg", ceea ce i-a făcut pe mulți oameni să facă greșeala de a crede că electronii și alte lucruri de acest gen sunt într-adevăr "undeva", dar că noi suntem doar nesiguri în mintea noastră. Această idee este greșită. Nu despre ea vorbea Heisenberg. A avea probleme în a măsura ceva este o problemă, dar nu este problema la care se referea Heisenberg.
Ideea lui Heisenberg este foarte greu de înțeles, dar o putem face mai clară cu un exemplu. În primul rând, vom începe să numim aceste grile "matrici", deoarece în curând va trebui să vorbim despre înmulțirea matricelor.
Să presupunem că începem cu două tipuri de măsurători, poziția (q) și impulsul (p). În 1925, Heisenberg a scris o ecuație ca aceasta:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=\sum _{a}^{}\,p(n,n-a)q(n-a,n-b)} (Ecuația pentru variabilele conjugate moment și poziție)
(Ecuația pentru variabilele conjugate moment și poziție)
El nu știa, dar această ecuație oferă un plan pentru a scrie două matrici (grile) și pentru a le înmulți. Regulile de înmulțire a unei matrici cu alta sunt un pic dezordonate, dar iată cele două matrici conform proiectului și apoi produsul lor:
Matricea de p
| Stări electronice | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| tranziție.... | ..... | ..... | ..... | ..... | |
Matricea de q
| Stări electronice | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| tranziție.... | ..... | ..... | ..... | ..... | |
Matricea pentru produsul celor două matrici de mai sus, așa cum este specificată de ecuația relevantă din lucrarea lui Heisenberg din 1925, este:
| Stări electronice | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Unde:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
și așa mai departe.
Dacă matricile ar fi inversate, ar rezulta următoarele valori:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
și așa mai departe.
Observați cum schimbarea ordinii de înmulțire modifică, pas cu pas, numerele care sunt efectiv înmulțite.