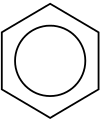
O hidrocarbură aromatică sau arenă este un compus cu inel de hidrocarbură. Are legături duble și simple alternante între atomii de carbon care formează inele. Mulți dintre acești compuși au un miros dulce, de unde și termenul "aromatic". Inelul de șase atomi de carbon din compușii aromatici este cunoscut sub numele de inel benzenic, după cel mai simplu inel de hidrocarbură posibil, benzenul (C6H6). Hidrocarburile aromatice pot fi monociclice (MAH) sau policiclice (PAH).
Unii compuși fără bază de benzen, numiți heteroarene, care respectă regula lui Hückel, sunt, de asemenea, compuși aromatici. În acești compuși, cel puțin un atom de carbon este înlocuit cu unul de oxigen, azot sau sulf (de exemplu: piridină, furani, tiofeni).
Structură și criterii de aromaticitate
Pentru ca un ciclu să fie considerat aromatic trebuie îndeplinite câteva criterii esențiale:
- Ciclicitate: atomii trebuie să formeze un inel închis;
- Conjugare: existența unui sistem π continuu (orbitali p de-a lungul inelului care se suprapun);
- Planaritate: molecula trebuie, în general, să fie plană sau aproape plană pentru a permite suprapunerea orbitalilor p;
- Regula lui Hückel: sistemul π trebuie să conțină 4n+2 electroni π (unde n = 0, 1, 2 ...). Aceasta explică stabilitatea aromatică: de exemplu, benzenul are 6 electroni π (n = 1).
Există și sisteme antiaromatice (care au 4n electroni π) și sunt instabile comparativ cu sistemele aromatice.
Clasificare
- Monociclice (MAH): conțin un singur inel aromatic, exemplu clasic fiind benzenul și derivații săi (toluenă, anilină).
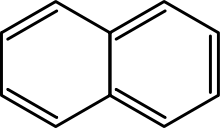
- Policiclice (PAH): conțin două sau mai multe inele fuzionate (de ex. naftalina C10H8, antracenul C14H10, fenantrena C14H10). PAH-urile pot avea proprietăți chimice și toxice distincte față de MAH.
- Heteroarene: inele aromatice care conțin heteroatomi (oxigen, azot, sulf). Exemple: piridină (C5H5N), furane (C4H4O), tiofene (C4H4S), pirrol (C4H5N).
- Arene condensate vs. necondensate: PAH-urile pot fi lineare (antracen) sau angular/condensate (fenantren), ceea ce influențează proprietățile fizice și reacțiile.
Exemple importante
- Benzen (C6H6) – modelul de referință pentru aromaticitate;
- Toluenă (C7H8) – benzen substituit cu grupă metil, folosit ca solvent;
- Naftalină (C10H8) – două inele fuzionate, folosită în industria organică;
- Antracen și fenantren – PAH-uri cu trei inele fuzionate;
- Piridină, furani, tiofeni – exemple de heteroarene cu aplicații în sinteză și în medicină.
Reactivitate și mecanisme caracteristice
Un tip comun de reacție al aromaticelor este substituția electrofilă aromatică (SEAr), în care un atom de hidrogen de pe inel este înlocuit de un nucleu electrofil (de ex. nitrării, sulfonări, halogenări, alchilări Friedel–Crafts). Aromaticitatea tindă să se mențină în astfel de reacții — inelul nu este de obicei rupt, ci doar substituit.
Unele reacții pot duce la pierderea aromaticității (ex. adiții) și sunt în general mai puțin favorabile din punct de vedere energetic. Heteroarenele pot avea reactivitate diferențiată în funcție de natura și poziția heteroatomului.
Proprietăți fizice și aplicații
- Mulți arenuri sunt compuși volatili, cu mirosuri caracteristice (benzen, toluen);
- Se folosesc pe scară largă ca solvenți, intermediari în sinteza chimică, materii prime pentru polimeri și coloranți;
- PAH-urile sunt componente ale funinginii și ale produselor de ardere incompletă (tone de hârtie, carburanti), iar unele au proprietăți semiconductoare utile în materiale organice.
Impact asupra sănătății și mediului
Multe PAH-uri sunt toxice și unele sunt cunoscute ca fiind cancerigene (de ex. benzo[a]piren). Ele se acumulează în mediu (sol, sedimente) și pot fi generate prin ardere incompletă a combustibililor fosili, a lemnului sau în industria petrochimică. Manipularea și expunerea necesită măsuri de protecție și monitorizare.
Note finale
Aromaticitatea este un concept central în chimia organică care explică stabilitatea, reactivitatea și proprietățile multor compuși organici. Deși termenul provine din mirosul unor substanțe, definiția modernă se bazează pe criterii electronice și structurale (conjugare, planaritate, regula lui Hückel) și se aplică unei game largi de sistemele ciclice atât hidrogenate cât și cu heteroatomi.