Modelul atomic Thomson
Modelul budincii de prune a fost un model timpuriu (și incorect) de atom din secolul XX. Acesta a fost propus de J.J. Thomson în 1904, după descoperirea electronului, dar înainte de descoperirea nucleului atomic. În acea perioadă, oamenii de știință știau că în atom exista o sarcină pozitivă care echilibra sarcinile negative ale electronilor, ceea ce făcea ca atomul să fie neutru, dar nu știau de unde provenea sarcina pozitivă. Modelul lui Thomson arăta un atom care avea un mediu sau un spațiu încărcat pozitiv, cu electroni încărcați negativ în interiorul mediului. La scurt timp după ce a fost propus, modelul a fost numit modelul "budincii de prune", deoarece mediul pozitiv era ca o budincă, cu electroni, sau prune, în interior.

Exemplu de model al lui Thomson
Evoluția în modelul atomic modern
Modelul lui Rutherford
Practic, în 1909, la scurt timp după ce modelul lui Thomson a fost propus, Hans Geiger și Ernest Marsden au făcut un experiment cu foi subțiri de aur, pentru a testa modelul lui Thomson. Profesorul lor, Ernest Rutherford, se aștepta ca rezultatele să dovedească faptul că Thomson avea dreptate, însă rezultatele au fost extrem de diferite de ceea ce se așteptau. În 1911, Rutherford a descoperit că sarcinile pozitive provin de la particule minuscule numite protoni, că protonii se aflau într-un centru minuscul numit nucleu și că electronii orbitau în jurul nucleului.
Modelul Bohr
Modelul lui Rutherford era destul de simplu, dar era greșit, deoarece electronii au sarcină și ar trebui să fie atrași de nucleul încărcat pozitiv. În 1913, Niels Bohr a adăugat "niveluri de energie" la modelul atomic. Electronii nu cad în nucleu, deoarece sunt conținuți în niveluri de energie, iar pentru a trece la niveluri de energie mai înalte este nevoie de energie suplimentară, iar pentru a trece la niveluri de energie mai joase este necesară o eliberare de energie. Nu este posibil să se schimbe stările energetice fără a schimba energia electronului. Dacă un electron este lovit de un foton (o particulă purtătoare de radiație electromagnetică), el va obține energie suplimentară și va trece la un nivel energetic superior (își schimbă starea), apoi va sări înapoi la un nivel energetic inferior, eliberând energia conținută. Acest nou model a fost numit modelul Bohr sau modelul Rutherford-Bohr. Acest lucru a adăugat o nouă ramură a științei: Fizica cuantică.
Modelul cuantic
În 1926, Erwin Schrödinger a folosit ideea că electronii acționează ca o undă, dar și ca o particulă, ceea ce este cunoscut sub numele de dualitatea undă-particulă. Acest lucru a adăugat un nou nivel la modelul atomic și la fizica cuantică. În cazul unei particule, puteți ști unde se află în spațiu dacă o observați (priviți). Dar în cazul unei unde, aceasta se află peste tot, astfel încât nu se poate defini unde se află exact. Acest lucru este cunoscut sub numele de incertitudine cuantică. În cazul unui electron, se poate cunoaște doar probabilitatea ca acesta să se afle într-un anumit loc, deoarece este o undă și o particulă. (A se vedea diagrama de mai sus)
O imagine care arată un electron care își schimbă nivelul de energie și care capătă și eliberează energie sub formă de fotoni.
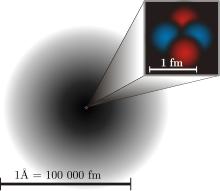
Aceasta arată modelul atomic actual. Umbrirea neagră din jurul atomului arată probabilitatea de a găsi un electron acolo. Cu cât este mai închisă, cu atât mai multe șanse de a găsi un electron în acel loc.
Pagini conexe
- Teoria atomică
- Mecanica cuantică
- J. J. J. Thomson
- Ernest Rutherford
- Niels Bohr
- Erwin Schrödinger
Căuta în