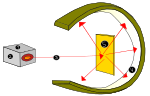
În 1850, Sir William Crookes a construit un "tub de descărcare", adică un tub de sticlă fără aer și cu electrozi metalici la capete, conectat la o sursă de înaltă tensiune. Atunci când se creează un vid în tub, se poate observa o descărcare luminoasă care trece de la catod (electrod încărcat negativ) la anod (electrod încărcat pozitiv). Crookes a denumit această emisie "raze catodice".
După experimentele cu raze catodice, Sir Joseph John Thomson a stabilit că raza emisă era formată din sarcini negative, deoarece acestea erau atrase de polul pozitiv. Thomson știa că atomii sunt neutrii din punct de vedere electric, dar a stabilit că, pentru ca acest lucru să se întâmple, un atom trebuie să aibă aceeași cantitate de sarcini negative și pozitive. Sarcinile negative au fost denumite electroni (e-).
Conform ipotezelor stabilite cu privire la sarcina neutră a atomilor, Thomson a propus primul model atomic, care a fost descris ca o sferă încărcată pozitiv în care electronii erau încastrați (cu sarcini negative). Acesta este cunoscut sub numele de modelul budincii de prune.
În 1906, Robert Millikan a determinat că electronii au o sarcină Coulomb (C) de -1,6 * 10−19, ceea ce a permis calcularea masei sale minuscule, egală cu 9,109 * 10 −31kg.
În același timp, experimentele efectuate de Eugene Goldstein în 1886 cu ajutorul tuburilor cu descărcare catodică i-au permis să stabilească faptul că sarcinile pozitive au o masă de 1,6726 * 10 −27kg și o sarcină electrică de +1,6 * 10 C−19. Lordul Ernest Rutherford a numit ulterior aceste particule încărcate pozitiv protoni