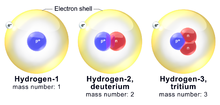
Atomii unui element chimic pot exista în diferite tipuri care au un comportament foarte asemănător, dar cântăresc cantități diferite. Aceștia se numesc izotopi ai elementului respectiv. Atomii aceluiași element au același număr de protoni, dar diferiți izotopi au numere diferite de neutroni. Diferiți izotopi ai aceluiași element au mase diferite, deoarece au un număr diferit de neutroni. Masa este cuvântul care desemnează cantitatea de substanță (sau materie) pe care o are un element. Lucrurile cu mase diferite au, de asemenea, greutăți diferite.
Unii izotopi nu sunt stabili, astfel încât se transformă în alt izotop sau element prin dezintegrare radioactivă. Aceștia se numesc izotopi radioactivi. Alții nu sunt radioactivi. Aceștia se numesc izotopi stabili.
Atomii aceluiași element au același număr de protoni, care se numește număr atomic. Diferiți izotopi ai unui element au numere diferite de neutroni. Prin urmare, aceștia au, de asemenea, numere de masă diferite, care reprezintă numărul de protoni plus numărul de neutroni. De obicei, un izotop este denumit prin indicarea elementului și a numărului de masă. De exemplu, simbolul pentru carbon este C și toți atomii de carbon au 6 protoni. Cel mai comun izotop al carbonului are, de asemenea, 6 neutroni, ceea ce îi conferă un număr de masă de 12 și se scrie carbon-12 sau12 C. Izotopul de carbon care are 8 neutroni se scrie carbon-14 sau14 C.
Cuvântul "izotop", care înseamnă "în același loc", provine de la faptul că izotopii aceluiași element se află în același loc în tabelul periodic.