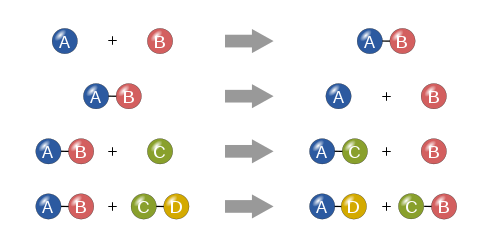
Sinteză
În cadrul unei reacții de sinteză, două sau mai multe substanțe simple se combină pentru a forma o substanță mai complexă.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB} 
"Doi sau mai mulți reactanți care dau un produs" este un alt mod de a identifica o reacție de sinteză. Un exemplu de reacție de sinteză este combinarea fierului și a sulfului pentru a forma sulfură de fier(II):
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS} 
Un alt exemplu este hidrogenul gazos simplu combinat cu oxigenul gazos simplu pentru a produce o substanță mai complexă, cum ar fi apa.
Descompunere
O reacție de descompunere are loc atunci când o substanță mai complexă se descompune în părțile sale mai simple. Este, așadar, opusul unei reacții de sinteză și poate fi scrisă astfel:
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B} 
Un exemplu de reacție de descompunere este electroliza apei pentru a obține oxigen și hidrogen gazos:
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}}}. 
Înlocuire unică
Într-o reacție de înlocuire unică, un singur element necombinat înlocuiește un alt element dintr-un compus; cu alte cuvinte, un element schimbă locul cu un alt element dintr-un compus Aceste reacții se prezintă sub forma generală de:
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} 
Un exemplu de reacție de deplasare unică este atunci când magneziul înlocuiește hidrogenul în apă pentru a produce hidroxid de magneziu și hidrogen gazos:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}}} 
Dublă înlocuire
Într-o reacție de dublă înlocuire, anionii și cationii a doi compuși își schimbă locul și formează doi compuși complet diferiți. Aceste reacții sunt de forma generală:
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB} 
De exemplu, atunci când clorura de bariu (BaCl2 ) și sulfatul de magneziu (MgSO4 ) reacționează, anionul SO42− schimbă locul cu anionul 2Cl−, dând compușii BaSO4și MgCl 2.
Un alt exemplu de reacție de dublă deplasare este reacția nitratului de plumb(II) cu iodura de potasiu pentru a forma iodură de plumb(II) și nitrat de potasiu:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}