CRISPR este un termen din domeniul cercetării ADN. Acesta înseamnă "clustered regularly-interspaced short palindromic repeats". Acestea fac parte din codul genetic la procariote: majoritatea bacteriilor și arheilor le au. Este apărarea lor împotriva atacului virușilor. Structura și funcția sa au fost descoperite în secolul XXI.
CRISPR are o mulțime de secvențe scurte și repetate. Aceste secvențe fac parte dintr-un sistem imunitar adaptiv pentru procariote. Le permite acestora să își amintească și să contracareze bacteriofagii care îi atacă. Ele funcționează ca un fel de imunitate dobândită pentru bacterii.
Aceștia pot modifica genele aproape oricărui organism. Acestea sunt utilizate de cercetători ca instrument de tăiere și inserție a genelor în modificarea genetică (MG). În prezent, se lucrează pentru a afla cum pot fi utilizate pentru a ataca bolile virale la om (terapie genică).
Structură și componente
Sistemul CRISPR este alcătuit, în principal, din trei elemente complementare:
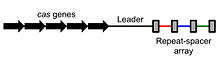
- Regiunile CRISPR — serii de repetiții scurte (repeats) separate de segmente non-repetate numite spacers. Spacer-ele provin din fragmente de ADN viral încorporate anterior și constituie „amintirea” infecțiilor anterioare.
- Gene cas (CRISPR-associated genes) — codifică proteinele Cas (de exemplu Cas9, Cas12, Cas13) care recunosc și taie ADN sau ARN țintă. Aceste proteine efectuează operațiunile efective de tăiere și procesare a ARN-urilor.
- ARN-ul CRISPR — transcrisele CRISPR (crRNA) care, împreună cu ARN-uri accesorii (de ex. tracrRNA în sistemele Cas9), direcționează proteinele Cas către secvența complementară din agentul patogen.
Mecanism de funcționare (pe scurt)
Sistemul funcționează în trei etape principale:
- Adaptare (acquisición) — la prima expunere la un virus, o bucată din ADN-ul viral este preluată și inserată ca spacer în regiunea CRISPR.
- Expresie și procesare — regiunea CRISPR este transcrisă într-un ARN lung care este procesat în fragmente scurte (crRNA) ce conțin spacer-ul viral.
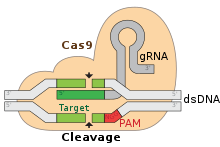
- Interferență — crRNA-ul, asociat cu proteina Cas, recunoaște secvența virală complementară și Cas taie ADN-ul/ARN-ul țintă, inactivând astfel invadatorul.
Un element important pentru recunoaștere este secvența PAM (protospacer adjacent motif) — o mică secvență din vecinătatea țintei necesară pentru ca anumite proteine Cas (de ex. Cas9) să acționeze.
Tipuri de sisteme CRISPR și proteine Cas
- Cas9 — cel mai cunoscut; taie ADN dublu-catenar și a fost folosit pe scară largă pentru editare genomică. Dezvoltat pentru uz simplu și eficient (Doudna & Charpentier).
- Cas12 — poate tăia ADN și are activitate trans-cleavage care a fost folosită în metode diagnostice.
- Cas13 — țintește ARN-ul, util pentru blocarea expresiei genice și pentru detectarea ARN-urilor virale.
- Editorii de bază și prime editing — tehnologii derivate care permit modificări precise de bază fără a produce întreruperi dublu-catenare majore; promit editări mai fine și cu mai puține efecte off-target.
Aplicații practice
CRISPR a revoluționat biologia moleculară și are aplicații foarte diverse:
- Cercetare fundamentală — generarea rapidă de linii celulare și modele animale cu gene knockout sau cu mutații specifice, pentru a studia funcția genelor.
- Medicină — terapii genice ex vivo (de exemplu corectarea celulelor stem hematopoietice pentru anemii hemolitice precum drepanocitoza și talasemia) și studii in vivo pentru boli monogenice, boli oculare sau cancer.
- Diagnostic — platforme precum SHERLOCK și DETECTR (bazate pe Cas13/Cas12) permit detectarea rapidă și sensibilă a ARN/DNA viral (util în diagnosticul infecțiilor).
- Agricultură — dezvoltarea soiurilor rezistente la dăunători, tolerante la stres sau cu caracteristici nutriționale îmbunătățite, adesea fără markerii clasici de transgenie.
- Biotehnologie industrială — optimizarea microorganismelor pentru producția de medicamente, enzime sau biocombustibili.
Limitări, riscuri și dezbateri etice
- Off-target — tăierile nedorite la alte locuri din genom pot cauza efecte adverse; metode mai noi reduc, dar nu elimină complet acest risc.
- Provocări de livrare — dificil de furnizat sistemul CRISPR eficient și sigur în anumite țesuturi (ex.: creier, mușchi), mai ales in vivo.
- Răspuns imun — organismele pot dezvolta anticorpi împotriva proteinelor Cas de origine bacteriană.
- Aspecte etice — editarea germinală (modificări transmise urmașilor) ridică preocupări serioase; cazul criogenării embrionilor modificați genetic (He Jiankui, 2018) a stârnit controverse și reglementări stricte.
Istorie și perspective
Secvențe CRISPR au fost observate pentru prima dată în anii 1980, dar funcția lor ca sistem imunitar adaptiv a fost demonstrată în anii 2000. În 2012, Emmanuelle Charpentier și Jennifer Doudna au descris modul în care sistemul CRISPR-Cas9 poate fi adaptat pentru a edita genomic, lucru răsplătit cu Premiul Nobel pentru Chimie în 2020. De atunci, tehnologia a evoluat rapid, cu multiple aplicații clinice emergente și numeroase studii în curs.
Concluzie
CRISPR reprezintă una dintre cele mai puternice unelte de editare genetică dezvoltate până în prezent: este precisă, relativ simplu de folosit în laborator și extrem de versatilă. Totuși, utilizarea ei în clinică necesită prudență, evaluări de siguranță riguroase și dezbateri etice bine fundamentate. Viitorul aduce probabil ediții mai sigure și mai selective (de ex. base editors, prime editors) și extinderea aplicațiilor în medicină, agricultură și diagnostic.