Termodinamică
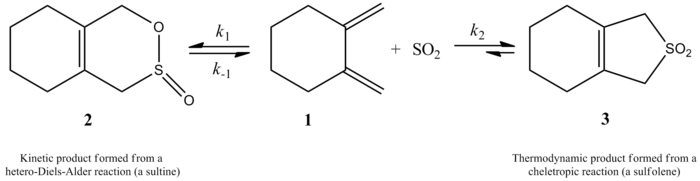
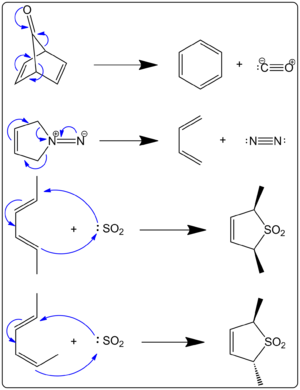
Atunci când dioxidul de sulf reacționează cu butadiena și izoprenul, rezultă două produse diferite. Mecanismul de reacție va controla ceea ce se obține. Sunt posibile atât un produs cinetic, cât și un produs termodinamic. Produsul termodinamic se obține mai mult decât produsul cinetic. Produsul cinetic provine dintr-o reacție Diels-Alder, în timp ce o reacție cheletropică produce un produs mai stabil din punct de vedere termodinamic. Calea cheletropică este utilizată mai mult pentru că produce un produs de adaos mai stabil cu cinci cicluri cu cinci membri. Schema de mai jos arată diferența dintre cei doi produși. Calea din stânga arată produsul termodinamic, în timp ce calea din dreapta arată produsul cinetic. Suarez și Sordo au demonstrat acest lucru în 1995. Ei au demonstrat acest lucru atât prin experimente, cât și prin calcule Gaussian.
Cinetică
Un exemplu în acest sens îl constituie reacțiile cheletrope ale 1,3-dienilor cu dioxidul de sulf. Chimiștii au analizat cu atenție cinetica acestei reacții. În 1976, Isaacs și Laila au măsurat factorii cinetici pentru adiția dioxidului de sulf la derivații butadienei. Vitezele de adiție au fost monitorizate în benzen la 30 °C cu un exces inițial de douăzeci de ori mai mare de dienă. Ei au folosit un spectrofotometru pentru a studia lumina la 320 nm pentru a măsura dispariția SO2 . Reacția a prezentat o "cinetică de pseudo-ordine întâi". Chimiștii au descoperit că grupările de retragere a electronilor de pe dienă au scăzut viteza de reacție. De asemenea, viteza de reacție a fost afectată considerabil de efectele sterice ale substituenților 2, grupurile mai voluminoase crescând viteza de reacție. (Cu alte cuvinte, cu cât grupul de atomi mai mare atârnat de al doilea atom de carbon era mai mare, cu atât reacția se desfășura mai rapid). Autorii atribuie acest lucru tendinței grupurilor voluminoase de a favoriza conformația cisoidă a dienei, care este esențială pentru reacție (a se vedea tabelul de mai jos). În plus, au fost măsurate vitezele la patru temperaturi pentru șapte dintre diene. Pe baza acestor măsurători, chimiștii au folosit ecuația Arrhenius pentru a calcula entalpia de activare (ΔH‡ ) și entropia de activare (ΔS‡ ) pentru fiecare reacție. Acesta a fost unul dintre primele eforturi importante de a studia cinetica unei reacții cheletrope.
| -Butadienă | 104 k /min−1 (30 °C) (± 1-2%) absolut | 104 k /min−1 (30 °C) (± 1-2%) relativ | ΔH‡ /kcal mol−1 | ΔS‡ /cal mol−1 K−1 |
| 2-metil | 1.83 | 1.00 | 14.9 | -15 |
| 2-etil | 4.76 | 2.60 | 10.6 | -20 |
| 2-izopropil | 13.0 | 7.38 | 12.5 | -17 |
| 2-terț-butil | 38.2 | 20.8 | 10.0 | -19 |
| 2-neopentil | 17.2 | 9.4 | 11.6 | -18 |
| 2-cloro | 0.24 | 0.13 | N/A | N/A |
| 2-bromoetil | 0.72 | 0.39 | N/A | N/A |
| 2-p-tolil | 24.7 | 13.5 | 10.4 | -19 |
| 2-fenil | 17.3 | 9.45 | N/A | N/A |
| 2-(p-bromofenil) | 9.07 | 4.96 | N/A | N/A |
| 2,3-dimetil | 3.54 | 1.93 | 12.3 | -18 |
| cis-1-metil | 0.18 | 0.10 | N/A | N/A |
| trans-1-metil | 0.69 | 0.38 | N/A | N/A |
| 1,2-dimetilen-ciclohexan | 24.7 | 13.5 | 11.4 | -16 |
| 2-metil-1,1,1,4,4-d4 | 1.96 | N/A | N/A | N/A |
Monnat, Vogel și Sordo, în 2002, au măsurat cinetica de adiție a dioxidului de sulf la 1,2-dimetilidencicloalcani. Aceștia au scris că reacția 1,2-dimetilidenciclohexanului cu dioxidul de sulf poate da doi produși diferiți în funcție de condițiile de reacție. Reacția produce sultina corespunzătoare printr-o reacție hetero-Diels-Alder sub control cinetic (≤ -60 °C), dar, sub control termodinamic (≥ -40 °C), reacția produce sulfolena corespunzătoare printr-o reacție cheletropică. Entalpia de activare pentru reacția hetero-Diels-Alder este cu aproximativ 2 kcal/mol mai mică decât cea pentru reacția cheletropică corespunzătoare. Sulfolena este cu aproximativ 10 kcal/mol mai stabilă decât sultina izometrică în soluție CH2 Cl2 /SO .2
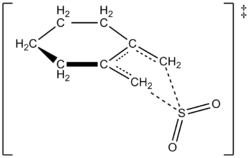
Autorii au reușit să elaboreze experimental o lege de viteză la 261,2 K pentru reacția 1,2-dimetilideneciclohexanului cu dioxidul de sulf pentru a obține sulfolenul corespunzător. Reacția a fost de ordinul întâi în cazul 1,2-dimetilidenciclohexanului, dar de ordinul doi în cazul dioxidului de sulf (a se vedea mai jos). Acest lucru a confirmat o predicție a chimiștilor teoreticieni bazată pe calcule cuantice ab initio de nivel înalt. Utilizând metode de calcul, autorii au propus o structură de tranziție pentru reacția cheletropică a 1,2-dimetilidenciclohexanului cu dioxidul de sulf (a se vedea figura din dreapta). Reacția este de ordinul al doilea în cazul dioxidului de sulf, deoarece o altă moleculă de dioxid de sulf se leagă probabil de starea de tranziție pentru a contribui la stabilizarea acesteia. Rezultate similare au fost găsite într-un studiu realizat în 1995 de Suarez, Sordo și Sordo, care au folosit calcule ab initio pentru a studia controlul cinetic și termodinamic al reacției dioxidului de sulf cu 1,3-diene.
d [ 3 ] d t = k 2 [ 1 ] [ S O 2 ] 2 {\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}} ![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)
Efectele solvenților
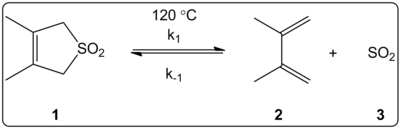
Efectul solventului asupra reacției cheletropice a 3,4-dimetil-2,5-dihidrotiofen-1,1-dioxid (prezentat în dreapta) a fost investigat cinetic în 14 solvenți. S-a constatat că constantele vitezei de reacție a reacției directe și inverse, precum și constantele de echilibru, sunt corelate liniar cu scara de polaritate a solventului ET (30).
Reacțiile au fost efectuate la 120 °C și au fost studiate prin spectroscopia 1H-NMR a amestecului de reacție. S-a constatat că viteza de reacție k1 scade cu un factor de 4,5 în cazul trecerii de la ciclohexan la metanol. S-a constatat că viteza inversă k-1 a crescut cu un factor de 53 de la ciclohexan la metanol, în timp ce constanta de echilibru Keq a scăzut cu un factor de 140. Se sugerează că există o schimbare a polarității în timpul procesului de activare, după cum reiese din relațiile dintre datele de echilibru și cele cinetice. Autorii spun că reacția pare să fie influențată de polaritatea solventului, iar acest lucru poate fi demonstrat prin schimbarea momentelor dipolare la trecerea de la reactant la starea de tranziție la produs. Autorii afirmă, de asemenea, că reacția cheletropică nu pare să fie influențată nici de aciditatea, nici de bazicitatea solventului.
Rezultatele acestui studiu îi determină pe autori să se aștepte la următoarele comportamente:
1. Schimbarea polarității solventului va influența viteza mai puțin decât echilibrul.
2. Constantele de viteză vor fi caracterizate de efectul opus al polarității: k1 va scădea ușor odată cu creșterea lui ET (30), iar k-1 va crește în aceleași condiții.
3. Efectul asupra k-1 va fi mai mare decât asupra k1 .

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)