Cinetica chimică, numită și cinetica reacțiilor, studiază viteza cu care se desfășoară reacțiile chimice. Aceasta include studierea modului în care diferite condiții, cum ar fi temperatura, presiunea sau solventul utilizat, afectează viteza unei reacții. Cinetica chimică poate fi folosită și pentru a afla informații despre mecanismele de reacție și stările de tranziție.
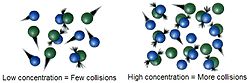
Ideea de bază a cineticii chimice se numește teoria coliziunii. Aceasta afirmă că, pentru ca o reacție să aibă loc, moleculele trebuie să se lovească între ele. Prin urmare, modalitățile de creștere a vitezei reacției trebuie să crească numărul de ciocniri. Acest lucru se poate face în mai multe moduri.
Prin experimente este posibil să se calculeze vitezele de reacție din care se pot obține legile de viteză și constantele de viteză. O lege de viteză este o expresie matematică cu ajutorul căreia puteți calcula viteza unei reacții, dată fiind concentrația reactivilor.