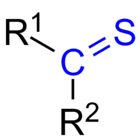
O tiocetonă (sau thionă) este orice moleculă cu grupul R2 C=S. Este ca o cetonă cu atomul de oxigen schimbat cu unul de sulf. Atomul de sulf are o legătură dublă cu atomul de carbon. De asemenea, acesta păstrează două perechi singuratice.
Tiocetonele sunt foarte reactive. Acest lucru se datorează faptului că sunt electrofile bune. Multe dintre ele sunt instabile. Ele doresc să formeze inele. Fac acest lucru prin reacții de cicloadiție, similare cu reacția Diels-Alder.
În cazul în care una dintre grupele R este hidrogen, molecula este versiunea cu sulf a unei aldehide. Se numește thial și este chiar mai reactivă decât o tiocetonă.
Structură electronică și proprietăți
Gruparea C=S este analogă grupării carbonil (C=O), dar prezintă diferenţe importante datorită proprietăților atomului de sulf: sulf are electronegativitate mai mică și orbitalele 3p nu se suprapun la fel de eficient cu orbitalul 2p al carbonului. Drept rezultat, legătura π C=S este mai slabă decât π C=O, ceea ce influențează stabilitatea și reactivitatea moleculei. De aceea, tiocetonele sunt adesea mai polarizabile și mai susceptibile la atacul nucleofililor „soft” (ex. sulfuri, tioli, fosfine).
Reactivitate tipică
- Adăugare nucleofilă: Tiocetonele pot suferi adăugări nucleofile la carbonul electrofil al grupării C=S; aceste adăugări sunt favorizate pentru nucleofili moi. În cazul thialelor (R–CH=S), reactivitatea este și mai mare, ducând la polimerizare sau la formarea rapidă de aducte cu nucleofili.
- Cicloadiții și formarea de inele: Multe tiocetone participă ușor la cicloadiții — de exemplu acționează ca dienofile în reacții de tip Diels–Alder pentru a da heterocicli sau pot forma aducte [2+2] cu alchene, în funcție de substrat și condiții. Această tendință de a "căuta" inele explică parțial instabilitatea multor tiocetone simple.
- Formarea derivatilor de tip thioacetal/thioketal: În prezența tioalcoolilor (RSH) sau a altor nucelofili care conțin sulf se pot obține compuși adăugați (analogi ai acetalelor, dar conținând sulf), utili în sinteză pentru protejarea sau transformarea grupării tiocarbonil.
- Reacții de oxidare și transformări: Tiocetonele pot fi transformate sau oxidate în produse diferite în funcție de reactivi; de asemenea, oxigenul sau alți agenți puternici pot conduce la desulfurare sau la schimbări ale structurii.
Sinteză
Tiocetonele se obțin frecvent prin thionare a cetonelor (înlocuirea atomului de oxigen cu sulf). Reactivi obișnuiți pentru această transformare sunt fosforul pentasulfid (P2S5) și reactivi comerciali mai blânzi, precum Lawesson's reagent. Alegerea reactivului, solventului și temperaturii influențează randamentul și stabilitatea produsului obținut; pentru tiocetone foarte reactive se lucrează adesea la temperaturi scăzute sau în prezența stericelor voluminoase care stabilizează produsul.
Stabilitate și factori de stabilizare
Stabilitatea unei tiocetone depinde de substituenți (R): grupările aromatice conjugate sau substituenții voluminoși pot stabiliza tiocetona prin delocalizare electronică sau prin protejarea sterică împotriva dimerizării și a atacului nucleofil. În schimb, tiocetonele cu substituenți electron-donatori puternici sau cu hidrogen (thialele) sunt de obicei mult mai reactive și adesea instabile la temperatura camerei.
Proprietăți spectroscopice și caracterizare
Tiocetonele prezintă tranziții electronice de energie mai mică comparativ cu cetonele omoloage, ceea ce le conferă adesea culoare intensă (multe tiocetone sunt colorate). În spectroscopie IR apare o bandă caracteristică atribuită vibrației C=S; poziția exactă depinde de structură, dar este diferită față de banda C=O. În 13C NMR, carbonul tiocarbonil afișează un semnal caracteristic, util pentru identificare; alte tehnici (UV–Vis, MS) completează caracterizarea.
Exemple și aplicații
Un exemplu cunoscut este thiobenzophenone (diphenyltiocetonă), care este colorată și folosită în studii de reactivitate ale tiocarbonililor. Tiocetonele sunt folosite ca intermediari în sinteze organice, în particular atunci când se urmărește formarea unor heterocicli sau introducerea de unități conținând sulf. Datorită reactivității lor selectate față de nucleofili „soft”, au aplicabilitate în chimia organosulfurică și în sintezele care necesită transformări regionale selectives.
Observații practice
- Lucrează cu tiocetone sensibile la temperatură la rece și în absența oxigenului, când este necesar.
- Folosește reactivi de thionare adecvați (ex. Lawesson's reagent) pentru a evita reacții secundare nedorite.
- Fii atent la manipulare: multe tiocetone și thialele sunt foarte reactive și pot fi toxice sau iritante.
În concluzie, tiocetonele (thionele) sunt analogi sulfurici ai cetonelor, cu proprietăți electronice și reactivitate distincte. Datorită legăturii C=S mai polarizabile și a orbitalelor sulfurului, ele sunt în general mai reactive decât cetonele și au un comportament chimic valoros în sinteza organică, deși necesită condiții adecvate pentru a fi manipulate în siguranță.